Science:影响牙周炎新型调节剂被发现——纤维蛋白
2022-01-04
分类:
研究进展
阅读(1416)
收藏
原文题目:Fibrin is a critical regulator of neutrophil effector function at the oral mucosal barrier
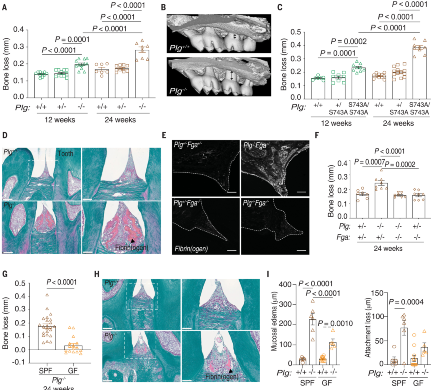
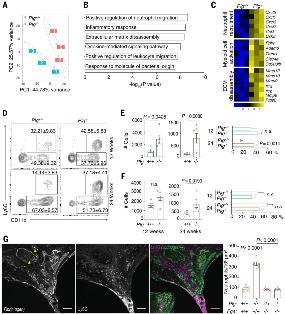
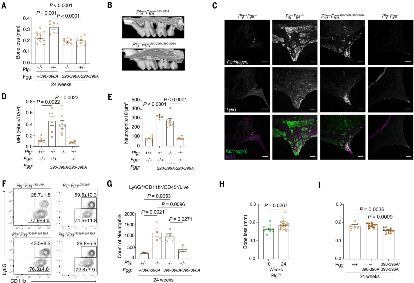
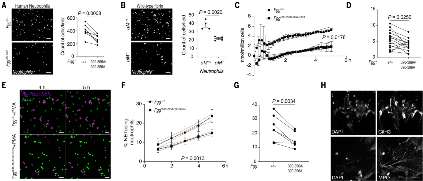
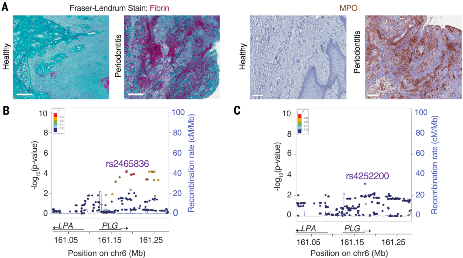
通讯作者: NIKI M. MOUTSOPOULOSDOI:10.1126/science.abl5450粘膜屏障部位持续暴露于各种环境刺激下,粘膜组织特异性免疫反应的微调是维持组织稳态的关键。然而,粘膜屏障免疫的具体机制仍有待阐明。在人类中,纤溶酶原(丰富的血浆蛋白酶纤溶酶的酶原形式)的先天性缺乏会导致严重的粘膜炎性疾病,包括口腔(木质化牙周炎)、眼部(木质化结膜炎)、肺、阴道和胃肠道,这表明纤溶酶在粘膜屏障稳态。纤维蛋白是纤溶酶的主要生理靶点,在人类和动物模型中与纤溶酶原缺乏相关的异常炎症反应与血管外纤维蛋白沉积有关。在口腔中,假设过量的血管外纤维蛋白是严重口腔粘膜(牙龈)炎症的基础,支持骨(牙周)破坏,以及与人类纤溶酶原缺乏相关的青少年牙列缺失。牙列周围的粘膜炎症和下方骨骼的破坏也是牙周炎常见形式的标志。在这项研究中,作者试图确定纤维蛋白沉积和口腔粘膜免疫病理学之间的机制联系。作者采用了一系列基因工程小鼠模型和药理学抑制剂,辅以人体组织学和遗传学研究,以探讨纤维蛋白沉积与局部免疫病理学之间的关联。与纤溶酶原缺陷人类的发现一致,纤溶酶原缺乏的小鼠表现出血管外纤维蛋白积聚、牙龈炎症和牙周骨质流失。纤维蛋白前体纤维蛋白原的遗传或药理学消除可防止纤溶酶原缺乏症的口腔免疫病理学,这证明了纤维蛋白在纤溶酶原缺乏相关的粘膜免疫病理学中的关键作用。图2:Plg缺乏症的黏膜免疫病理病变以中性粒细胞为主。值得注意的是,与特定的无病原体小鼠相比,纤溶酶原缺陷的无菌小鼠的口腔免疫病理学显着降低。这表明共生微生物群落是口腔黏膜纤维蛋白沉积和相关免疫病理学的触发因素。纤溶酶原缺陷小鼠的口腔病变是靠近纤维蛋白沉积物的嗜中性粒细胞积聚部位。值得注意的是,尽管具有未减弱的牙龈纤维蛋白沉积和中性粒细胞积累,但表达缺乏髓系整合素α M β 2结合位点的突变纤维蛋白的纤溶酶原缺陷小鼠并未发生牙周病。α M β 2 的纤维蛋白参与促进中性粒细胞效应功能,包括活性氧的产生和中性粒细胞胞外陷阱 (NET) 的形成 (NETosis)。因此,NETosis 的遗传或药理学消融减少了纤溶酶原缺陷小鼠的牙周骨破坏。因此,中性粒细胞激活,通过纤维蛋白 - 中性粒细胞的结合,触发口腔粘膜免疫病理学。在正常纤维蛋白溶解条件下,纤维蛋白-中性粒细胞结合的取消也减少了与年龄相关的牙周免疫病理,这表明该机制在非孟德尔牙周炎形式中具有更广泛的作用。与这个概念一致,人类PLG 的变异 编码纤溶酶原的基因与欧洲血统的美国人队列中常见的严重牙周病的患病率增加有关。中性粒细胞的稳态调节对于口腔内免疫系统的最佳功能至关重要。中性粒细胞向口腔黏膜的低募集和过度募集都与炎性牙周骨丢失有关。在中性粒细胞减少和中性粒细胞积聚的情况下,侵袭性牙周炎的发展揭示了在维持牙周健康中对精细平衡的中性粒细胞数量和中性粒细胞功能的要求。与中性粒细胞生成和生命周期缺陷相关的先天性疾病,例如骨髓衰竭综合征、严重的先天性中性粒细胞减少症和白细胞粘附缺陷,导致早发性牙周炎,而过多的中性粒细胞浸润和激活与非孟德尔形式的牙周病有关。图3:纤维蛋白(原)上的髓样整联蛋白 α M β 2结合基序介导纤溶酶原缺乏诱导的口腔免疫病理学。目前的研究清楚地证明,中性粒细胞募集增加本身不足以触发口腔内的免疫病理学。在这里,作者表明,招募到牙周环境中的中性粒细胞与局部沉积的纤维蛋白的结合对于充分执行关键的免疫病理学引发的中性粒细胞效应功能,包括 NETosis 是必不可少的。作者发现,即使由于纤维蛋白溶解受损导致牙龈组织内中性粒细胞的稳态水平大幅增加,也未能在经过基因改造以携带无法通过主要中性粒细胞整联蛋白 α M β 2与中性粒细胞结合的突变纤维蛋白的小鼠中引发免疫病理学。α M β 2 中的突变由于单核细胞、巨噬细胞和小胶质细胞活化的破坏,-结合基序保护自身免疫疾病模型中的纤维蛋白(原)相关免疫病理学,包括关节炎和多发性硬化症。然而,迄今为止,纤维蛋白引发的粘膜疾病和纤维蛋白-中性粒细胞介导的免疫病理学的潜在机制尚未得到很好的理解。图 4:纤维蛋白(原)-中性粒细胞相互作用通过 α M β 2结合触发关键的中性粒细胞效应功能。嗜中性粒细胞募集和激活,活性氧的产生,和NETosis都记载在患者组织活检与牙周炎。中性粒细胞的过度激活、ROS 的产生和 NET 的释放与多种炎症和自身免疫病理有关 ,并与关节炎引起的炎症性骨破坏有关。那么中性粒细胞如何被激活并参与牙周免疫病理学尚不完全清楚。在这里,作者提供了令人信服的证据,表明 NETosis 在纤溶缺陷的情况下部分负责介导口腔粘膜免疫病理学和牙周骨丢失。使用 NET 消耗的体内模型(Plg -/-;Ela -/-和Plg -/- -DNase I),作者证实 NETosis 在纤维蛋白诱导的粘膜免疫病理学中起重要作用。然而,通过 NET 抑制来挽救骨质流失并不完全,就像在Plg -/- 中一样;FGG 390-396A / 390-396A 小鼠,这表明除了 NETosis 之外,纤维蛋白介导的免疫病理学还有其他作用。研究人员提出如下假设,如果通过纤维蛋白 α M β 2结合位点激活中性粒细胞是一种生理保护机制,可以在损伤和炎症部位激活中性粒细胞并促进微生物清除。然而,在纤维蛋白溶解缺陷导致纤维蛋白积聚的情况下,可能其变得夸大并导致免疫病理学。这种机制与口腔黏膜特别相关,其中中性粒细胞不断迁移以执行稳态功能,即使在健康环境中也是如此。然而,纤维蛋白 - 中性粒细胞轴是否负责Plg中其他屏障(如胃肠道和眼表)的粘膜免疫病理学作者的研究没有探讨缺陷。众所周知,Plg缺乏症的粘膜疾病是由所有组织中的纤维蛋白积聚介导的 ,但尚不清楚中性粒细胞或其他位置相关的骨髓亚群结合α M β 2还是其他纤维蛋白介导的炎症途径致力于促进不同粘膜部位的免疫病理学。图 6:纤维蛋白-中性粒细胞轴作为常见牙周炎形式的引发剂消除纤维蛋白上的 α M β 2结合位点可以保护野生型小鼠免受自发性年龄相关牙周病的侵害,这表明通过纤维蛋白参与激活中性粒细胞效应器功能可能会导致患有牙周病和牙周病的个体发生牙周病。纤溶功能正常。在没有综合征性孟德尔疾病的情况下,人类遗传证据支持PLG在常见牙周炎形式中的作用。最近对牙周炎全基因组关联研究的荟萃分析显示,PLG多态性是侵袭性牙周炎的两个主要危险因素之一,其中包括近 15,000 名欧洲血统的成年参与者。较早的一项研究还强调了PLG下游的多态性是心血管疾病和牙周炎之间的共同遗传风险位点。与之前的工作一致,PLG是北美大量欧洲血统成年人中牙周炎的遗传风险因素。此外,PLG多态性与高水平的牙周病原体A.放线菌( Aa )密切相关,Aa是一种通常在侵袭性牙周病患者中检测到的微生物。与严重牙周炎相关的先导 SNP (rs2465836) 与最近欧洲侵袭性牙周炎研究中的先导标记 (rs1247559) 存在强连锁不平衡。此外,导致高Aa定植信号的 SNP (rs4252200)与先前报道的侵袭性牙周炎和心血管疾病相关的多态性 (rs4252120接近。PLG中常见多态性的功能作用的未来研究基因座对于确定有缺陷的纤维蛋白溶解是否是易感性的基础是必要的,并且可以在非综合征性牙周炎患者的一个子集中进行靶向。值得注意的是,这里发现的牙周病中纤维蛋白-中性粒细胞介导的炎症途径确定了该疾病的一个假定的新治疗靶点。为支持这一观点,一种靶向纤维蛋白α M β 2结合位点γ377 至 395的单克隆抗体最近在多发性硬化症动物模型中显示出治疗活性。总之,这项工作证明了纤溶酶介导的纤维蛋白溶解在口腔黏膜稳态和疾病中的重要作用,并表明靶向纤维蛋白 - 中性粒细胞参与可能有益于预防或治疗流行的人类疾病牙周炎。作者将纤维蛋白确定为口腔黏膜屏障稳态的关键免疫调节剂,由中性粒细胞的局部参与和激活介导。这些发现提供了对纤维蛋白在有缺陷和正常纤维蛋白溶解情况下中性粒细胞活化和口腔粘膜免疫中的作用的见解。该研究为理解纤维蛋白 - 中性粒细胞参与作为预防或治疗流行的人类疾病牙周炎的目标铺平了道路。https://www.science.org/doi/10.1126/science.abl5450